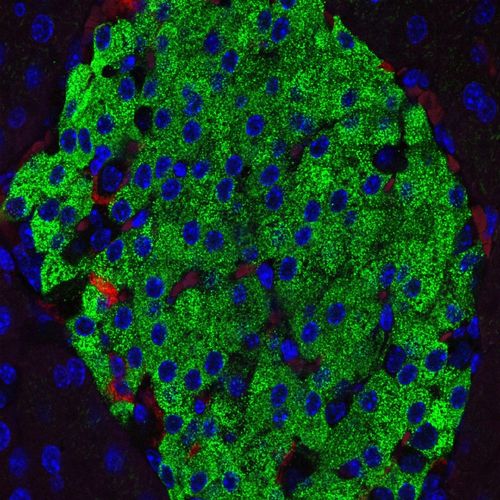
Die Bauchspeicheldrüse besteht zu einem Großteil aus Beta-Zellen. Sie produzieren das Insulin und schütten das Hormon ins Blut aus. Die Zellen sind in kleinen Zellhaufen organisiert, die wie Inseln im Gewebe verteilt sind. In diesen Langerhans-Inseln sind Forscher des Rudolf-Schönheimer-Instituts für Biochemie und des Carl-Ludwig-Instituts für Physiologie der Universität Leipzig nun auf besondere Rezeptoren gestoßen: „Bislang sind uns diese Rezeptoren eigentlich im Zuge der Ausprägung von Synapsen und neuronalen Netzwerken bekannt. Es hat uns sehr überrascht, dass sie noch eine ganz andere Funktion haben und zudem auch anders aussehen als im Gehirn“, sagt Dr. Simone Prömel, Gruppenleiterin am Rudolf-Schönheimer-Institut für Biochemie und Leiterin der Studie.
Zunächst untersuchten die Wissenschaftler den Rezeptor in einem Zellkulturmodell, später am Tiermodell, um auch primäre Zellen für die Studie nutzen. „Wir haben in beiden Kontexten zeigen können, dass mehr Insulin von den Zellen abgegeben wird, wenn der Rezeptor blockiert wird“, beschreibt Dr. Doreen Thor das Wirkprinzip. Dr. Thor ist ebenfalls Gruppenleiterin am Rudolf-Schönheimer Institut für Biochemie und Autorin der Studie. Dieses Ergebnis könnte der Therapie des Diabetes neue Möglichkeiten eröffnen. Die Forscher diskutieren in ihrer Publikation, dass dieser Rezeptor ein Angriffspunkt in der frühen Phase des Diabetes wäre. „Wir könnten diesen Rezeptor blocken, um mehr Insulin freizusetzen und den Blutzuckerspiegel schneller zu regulieren“, sagt Prömel. So könnten spezifische Antikörper oder andere Inhibitoren die Arbeit des Rezeptors modifizieren. Diese Möglichkeiten wollen die Wissenschaftler nun in weiteren Untersuchungen ausloten.
An der Leipziger Studie waren mehrere Einrichtungen der Medizinischen Fakultät der Universität Leipzig beteiligt: Rudolf-Schönheimer-Institut für Biochemie, Direktor Prof. Dr. med. Torsten Schöneberg, mit der Beteiligung des Carl-Ludwig-Institut für Physiologie, Geschäftsführender Direktor Prof. Dr. med. Jens-Karl Eilers. Sie wurde in Kooperation mit dem IFB AdipositasErkrankungen durchgeführt.
Originaltitel der Veröffentlichung in Cell Reports:
„Involvement of the Adhesion GPCRs Latrophilins in the regulation of insulin release”, DOI: doi.org/10.1016/j.celrep.2019.01.040